碳酸铜存在吗_水溶液中存在碳酸铜吗?
碳酸铜存在吗_水溶液中存在碳酸铜吗?
在文献的溶解性表中,标明水溶液中不存在CuCO3,而我国中学化学教材酸、碱和盐的溶解性表,仍标明CuCO3不溶于水。我们查阅了美国化学文摘、美国化学学会全文数据库和Elsevier全文数据库,尚未发现在水溶液中制得CuCO3,即在水溶液中CuCO3是不存在的。
在稀硫酸铜溶液中加入碳酸钠,析出沉淀是蓝色碱式碳酸铜[2CuCO3·3Cu(OH)2]。易溶性铜盐与NaHCO3溶液反应,析出的沉淀也是碱式碳酸铜,而不是碳酸铜。可由如下计算证明之:
0.10mol/LNaHCO3溶液的pH=8.3,即H+浓度是5.0×10-9mol/L,OH-浓度是2.0×10-6mol/L。
当Cu2+浓度和HCO-3浓度都是0.10mol/L时,生成Cu(OH)2的离子积是4.0×10-3,大于其溶度积5.6×10-20,故可生成Cu(OH)2沉淀。在水溶液中NaHCO3发生水解和电离反应:
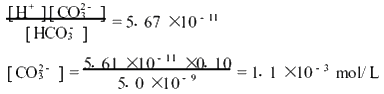
HCO-3+H2O=H2CO3+OH- (2)
HCO-3=H++CO2-3 (3)
由于298K时,HCO-3的水解常数是2.33×10-8,电离常数是5.67×10-11,它们的数值都很小,所以据反应(3)计算CO2-3的浓度时,可忽略水解和电离反应所消耗HCO-3的浓度。由反应(3)可求得0.10mol/LNaHCO3溶液中的CO2-3的浓度:
由计算所得到CuCO3(晶体)的标准生成自由能ΔfG298°=-517.5kJ/mol,Cu2+(aq)的ΔfG298°-64.9kJ/mol,
CO2-3(aq)的ΔfG298°=-527.6kJ/mol,可求得298K时,Cu2CO3(晶体)的Ksp=2.5×10-10。这个数值与参考文献中的数据完全相同。
当Cu2+浓度和HCO-3浓度均为0.10mol/L时,生成Cu2CO3的离子积是1.1×10-4,大于其溶度积2.5×10-10,故可能生成CuCO3沉淀。在这个溶液中同时可析出Cu(OH)2和CuCO3,因此,所析出的沉淀是碱式碳酸铜,而不是CuCO3。
在铜(Ⅱ)盐溶液中加入碳酸氢钠溶液,只能得到碱式碳酸铜沉淀。硫酸铜溶液与Na2CO3和NaHCO3混合溶液反应,pH=5.68时,得到的产物是碱式碳酸铜[。pH=8.3时,Na2CO3已全部转变成NaHCO3。这也说明易溶性铜盐(Ⅱ)与NaHCO3溶液反应,析出的沉淀亦是碱式碳酸铜。
综上所述,说明在水溶液中不存在CuCO3。建议将中学化学教材的酸、碱和盐溶解性表中CuCO3不溶于水,改成在水溶液中不存在。
https://m.oubohk.cn/yuwen/59857/

